Еще 12 лет назад Бразилия стала планетарным лидером в использовании технологии in vitro, на ее долю приходилось 86% (!) мирового производства «пробирочных» эмбрионов.
В прошлом году, отдавая дань успехам бразильских эмбриологов, европейская ассоциация ТЭ (АЕТЕ) выпустила совместный с бразильским сообществом специалистов ТЭ (SBTE) сборник статей в бразильском журнале Animal Reproduction (Official journal of the Brazilian College of Animal Reproduction, v.16, n.3 July/September 2019) [5]. Важно, что его содержимое описывает задачи и пути их решения, которые ставят перед современной эмбриологией производители мяса и молока. Заглядывает на десятилетие вперед и призывает быть готовым к этим переменам.
Минимум научной «воды», максимум применения ТЭ для повышения качества репродукции коров и телок в промышленном скотоводстве. Чем живет современная ТЭ?
Полистаем его, чтобы понять тенденции, заботы, задачи и пути их решения европейскими и бразильскими учеными-эмбриологами и сразу «порадуемся» тому факту, что на фермы Бразилии срочно требуется 4000 ветеринаров (с. 364). А мы то думали, что это только наша проблема.
ТАI (с. 368). В настоящее время применение программ синхронизация овуляции + ИО в заданное время (программа Time AI, TAI) в Бразилии охватывает 86% поголовья-ИО или 13.3 млн. процедур в год (в 2002 году — лишь 1% покрываемого поголовья). В среднем при ТАI тратят 2.4 и 1.4 доз семени на одну племенную самку молочной и мясной породы.
Первые протоколы по осеменению TAI для крупного рогатого скота появились в середина 1990-х годов с использованием протокола Овсинч (GnRH — 7 дней / PGF — 48 часов / GnRH – 16 часов до ИО; Pursley et al., 1995). В настоящее время программы ТАI претерпели различные модификации, чтобы облегчить управление и улучшить показатели беременности. В Бразилии, для TAI часто используют протокол на основе эстрадиола (E2) и прогестерона (P4) (Baruselli et al., 2002; Sá Filho et al., 2009; Baruselli et al., 2012). Время использования внутриматочного устройства с прогестероном (P4) может отличаться от 5 до 9 дней.
Многие протоколы были разработаны для разных пород, категорий животных и для разных скотовладельцев, чтобы адаптировать лучшие репродуктивные программы для промышленной фермы. Тем не менее многие из этих протоколов используются примерно с одинаковой эффективностью.
Рост популярности программы ТАI у животноводов Бразилии за последние 16 лет оценивается в 130 раз (!) со 100 тыс. протоколов в 2002 г. до 13.9 млн. процедур в 2018 (86% ИО) в стадах скота молочного и мясного направления (Baruselli 2019). Сегодня бразильцы массово переводят промышленное животноводство на синхронизированное ИО и ТЭ.
Не устану повторять – вот вам и развивающаяся страна третьего мира! Как говорил М. Жванецкий: хочешь осеменить корову – произвел укол, хочешь вызвать овуляцию – произвел другой укол, не произвел – не осеменишь. Мир сошёл с ума или это дань прогрессу?
ТЕТ (с. 370). После отработки программ ТAI бразильцы перешли к программам фиксированного времени ТЭ на реципиентах (ТЕТ), используя те же программы синхронизации, что и для ТАI. Такой прием синхронизации овуляции позволяет значительно увеличить число реципиентов под пересадку, делает ТЭ простой и доступной для мясных и молочных стад. Причем, по заверению разработчиков, в этом случае не требуется выявления охоты реципиентов, а ТЭ проводиться лишь по наличию желтого тела в яичниках. Эффективность синхронизации составляет 75-85% реципиентов (Baruselli et al., 2010).
Последующая услуга (ИО или ТЭ) оказывалась по наличию перегула реципиента или после исключения стельности УЗИ-доплером на 21-22 день.
В отличие от ТАI программы ТЕТ позволяют удержать требуемую фертильность по стаду в период теплового стресса на фермах (Baruselli и др., 2010). Мы об отечественном опыте борьбы с климатической яловостью в Краснодарском крае рассказывали в первой части обзора [1]. С первоисточником можно ознакомиться по ссылке [6]. Главное правило такой борьбы – заготовку эмбрионов проводить в комфортный для коров-доноров период, а ТЭ — в условиях теплового стресса, вместо планового ИО.
Не отмечено различий (76-80%) в эффективности использования совместных репродуктивных программ на коровах: TAI+ТАI (два синхронных ИО подряд) и TAI + TET. Оба приема оказались одинаково хороши (стельность 76-80%). Но у ТЕТ сексированными эмбрионами есть уже то преимущество, что она позволяет заказывать пол будущего теленка, тогда как TAI такого преимущества на коровах не имеет.

Уровень стельности после первого и второго подхода и совокупный процент стельности у 634 коров Nelore (Bos indicus), подвергшиеся воздействию четырех репродуктивных приемов, Martins et al., (2014).
Однако две ТЭ подряд (2 ТЕТ) дали снижение стельности в итоге до 56%. Эмбрионы в этом исследовании были происхождения in vitro и пересаживались свежеполученными.
Хотите продолжить до полного покрытия стада? Предлагается оптимальная схема интенсификации воспроизводства, опробованная на 360 лактирующих коровах породы нелоре: ТЭ + 2 ТАI. После первого подхода (ТЕТ) уровень беременности составил 44.2%, затем ТАI — 55.7% и еще TAI — 47.1%. Общий итог за 64-дневный сезон – 86.9% пересаженных и осемененных коров-реципиентов. Кажется – совсем неплохо!
С программой подготовки реципиентов по программе ТЕТ мы впервые познакомились (сами того не подозревая) еще в 2009 году в агрофирме «Калининская», Челябинской области, когда после канадских специалистов досаживали партию из 300 эмбрионов чистопородного герефорда, закупленных в Канаде. ТЭ выполняли телкам брединского типа методом direct transfer (без оценки эмбрионов) после оттаивания соломин в водяной бане. Подробности в «Животноводство России», 2011, №10 [7,8]. Еще 10 лет назад автор удивлялся отечественной селекции – надо было выводить за государственный счет новый брединский тип, регистрировать его и принимать поздравления научной общественности, чтобы потом использовать свое «брединское» творение как суррогатную мать.

Телята-ТЭ породы герефорд с реципиентами брединского типа, 2009
Тогда, 10 лет назад к реципиентам (на фото) претензий не было. Поставило в тупик другое — животноводы агрофирмы не предоставили списки синхронизированных телок в охоте по дням (как это принято при традиционной подготовки реципиентов). Мы привыкли подбирать возраст эмбрионов к сроку прихода в охоту реципиента на 7 или 8 день + определять наличие желтого тела в яичниках.
На наше недоумение по этому поводу был ответ, что канадцы выявлять охоту не просили, а после применения к животным схемы синхронизации охоты сажали эмбрионы лишь по наличию желтого тела у реципиентов в фиксированное время. Так автор впервые 10 лет назад вышел на производственное использование программ синхронизации овуляции и ТЕТ, которое уже тогда использовали продвинутые канадские эмбриологи.
Пришлось подчиниться пересадке без списков охоты, но и результат такой ТЭ в фиксированное время был невысок, около 34%. Поэтому к подготовке реципиентов по программе ТЕТ можно относиться скептически, особенно на небольших фермах. Почему бы одновременно с обещанной фиксированной овуляцией не определять время прихода реципиентов в охоту и подбирать их для ТЭ соответственно возрасту имеющихся эмбрионов в коридоре ±12 час. На мой взгляд – одно-другому не мешает.
Кстати, сегодня «калининские» герефорды, предки завезенных десять лет назад в виде эмбрионов из Северной Америки, пользуются хорошим спросом, чего не скажешь о брединском симментале отечественной селекции. Канадцы сразу решили — в суррогатную мать их!

Герефорды-красавцы из а/ф «Калиниская» Челябинской обл.
Быки-производители-ТЭ из «Калининской» пошли на продажу (в основном в Казахстан), в том числе и через аукционы, благодаря чему затраты на покупку и ТЭ были в значительной мере погашены [9], а вот логического продолжения по вымыванию эмбрионов герефордов канадской селекции и их реализации, к сожалению не последовало.
Надо ли заморачиваться с «таями» и «тетами» российскому производителю мяса и молока? Бразильские специалисты в этом материале считают, что в условиях своей страны – да, особенно на крупных фермах по производству мяса и молока. «These programs are currently established and present a positive economic return (Baruselli et al., 2018), generating higher meat and milk production per area and more value for the beef and dairy production chain» [5].
Одна из причин этого – громадное поголовье, с которым без «автоматизации» интенсивного воспроизводства просто не справиться. Несмотря на успехи последнего десятилетия в репродукции скота, только 13% бразильских коров и телок были ИО, по сравнению с 20-22% в мире (Thibier and Wagner, 2002; Vishwanath et al., 2003). Синхронизация в промышленном масштабе позволяет получать «положительную экономическую отдачу, обеспечивает рост производства мяса и молока на единицу площади и облегчает выполнение технологического цикла в производстве мяса и молока».
А что у нас? В доступной печати автор не нашел примеров производственного применения комплексных программ ТАI и ТЕТ на промышленных гигантах производства мяса и молока, таких как «Мираторг», «ЭкоНива» и др. Хотя отдельные элементы «синков» (овсинх, пресинк и др,) на них наверняка используются.
По-сути «синки» в отличие от традиционных схем синхронизации охоты (с простагландином F2α и прогестероном) синхронизируют овуляцию. Разные виды схем отличаются разной сложностью и стоимостью: от 3-х укольных Овсингов до навороченных Хит-синков и двойных Овсингов с шестью (!) уколами. Их применяют в зависимости от продвинутости ветврачей и технологических возможностей. Каждый выбирает для себя. Главная цель такой игры с гормонами – поймать фолликулярную волну в яичниках, синхронизировать ее прилив по стаду и обеспечить одновременную овуляцию у животных с одновременным их поголовным осеменением «вслепую» или последующей ТЭ по желтому телу [10].
Стоимость курса простенькой стимуляции/синхронизации охоты одного животного составляет $8-10. Теперь умножим ее к примеру, на 100 голов ежемесячных «синков»… Не дороговато ли платить по $1000 (75 тыс. руб.) в месяц за возможность ИО коров вслепую. Может быть целесообразней оснастить ферму автоматическим фиксатором охоты и/или добавить в штат техника ИО? Хотя, конечно, надо считать. Приверженцы «синков» полагают, что их использование сокращает сервис-период по стаду и по эффективности приближается к ИО в естественной охоте. Надо считать и проверять…
Какая существует альтернатива промышленной синхронизации ИО и ТЭ? Возможен ли обратный ход? На многих современных комплексах (в т.ч. и «Чебомилк») применяется программа автоматического выявления коров в спонтанной охоте, которая в ежесуточном режиме и бесплатно фиксируют эструс у животных (в %) и через автоматические ворота предоставляют их к услугам техников ИО.
На небольших и приближенных к природным условиям фермах гонадотропины, простагландины и прогестерон-содержащие средства применяют в основном для стимуляции гипофункциональных яичников, лечения кист и персистентных желтых тел, то есть используют преимущественно в лечебных целях.
В стадах половозрелых телок, телок-реципиентов и коров-доноров, которые лишены автоматического выявления охоты в помощь техникам ИО привлекают быков-пробников, которые являются еще и бесплатным мужским природным стимулятором (об этой практике использования бычков-пробников в «Чебомилке» в следующей части).
Да и в применении синхронизируюших охоту средств советские эмбриологи – не лыком шиты. При назначении графика ТЭ на выезде, массовых пересадках (в т.ч. и импортных эмбрионов), мы еще несколько десятилетий назад, использовали старую добрую схема синхронизации из 1 или 2-х инъекций (с интервалом в 11-14 дней) отечественного простагландина PGF2α, приводящая в охоту 50 или 80% животных соответственно.
Еще в прошлом тысячелетии («Молочное и мясное скотоводство» 2000, №7) мы ее усовершенствовали и довели до 3-х введений PGF2α в течение 33 рабочих дней, которые использовали для программной ТЭ из США и Канады [11].
В настоящее время мы ее применяем в лаборатории ТЭ «Чебомилк» и украсили дополнительным введением рилизинг-гормона (выделено красным) одновременно с первой инъекцией PGF2α. Суть такой добавки рилизинг-гормона в первую инъекцию PGF2α состоит в том, что каждый из препаратов (PGF2α или ГнРГ) находит свою мишень в яичниках (желтое тело или фолликул соответственно) и позволяет повысить первый приход животных в охоту до 60%.
Остальные 40% реципиентов будут попадать под пересадку после второй инъекции PGF2α и «гулять» под вторую ТЭ. К ним же будут добавлены телки, которые не подошли на первую пересадку из-за отсутствия желтого тела спустя 7 дней — им выполняется вторая инъекция ГнРГ. После второй ТЭ телкам которые не проявили охоту выполняли третье введение PGF2α, а телкам без желтого тела вновь выполняли ГнРГ.
Такая мульти-синхронизация позволяет за 3 раза и 32-35 дней пересадить до 95% первоначального стада телок-реципиентов.

- В первый день (= 0) выполняют введение PGF2α + ГнРГ (5 мл сурфагона), в охоту приходит до 60% реципиентов. Проводят первую ТЭ на 9-10 дн.
- На 11-14 день повторяют введение PGF2α животным, не пришедшим в охоту после первого введения PGF2α. А реципиентам, не подошедшим под ТЭ-1 из-за отсутствия желтого тела выполняют вторую инъекцию ГнРГ.
- Далее — выявление охоты и ТЭ-2. Избежавшим пересадки телкам выполняют третье введение ГнРГ, а телкам, не имевшим охоты после PGF2α-2 выполняют третью инъекцию PGF2α с последующей ТЭ-3.
«Опасение, что после эструса. индуцированного неоднократным введением PGF2α снизится приживляемость эмбрионов по сравнению со спонтанной охотой реципиентов, необоснованно. Напротив, по нашим данным, стельность реципиентов после первого, второго и третьего введения эструмата (257, 1383 и 41 гол ) составила соответственно 48, 56 и 56 %. У 88 телок, выявленных в спонтанной охоте, стельность после пересадки зарегистрировали в 55 % случаев» [11].
Надо добавить, что ректогенитальное обследование телок-реципиентов перед первым введением ГнРГ+PGF2α (в день = 0) на наличие желтого тела в яичниках позволит выполнять инъекции этих средств целенаправленно и по назначению, сэкономит расход препаратов, хотя и прибавит трудоемкости в осуществление программы синхронизации.
Применение процедур экстракорпорального оплодотворения ооцитов (ЭКО) коров молочных пород в Северной и южной Америке нарастает в геометрической прогрессии [5]. А вот Европа до сих пор считает, что американские «пробирочники» с их гигантоманией сбились с верного «путя» и предпочитают традиционные приемы ТЭ. Каких еще новостей ждать от репродуктивных технологий в скором времени?
1. Геномный анализ: от отбора животных до ооцитов и оценки эмбриона (396).
Экономический интерес геномной селекции животных состоит в возможности удвоить скорость генетического прогресса для выбранных признаков. Генетическое улучшение происходит за счет повышенная точности определения генетической ценности уже для молодых животные (Wiggans et al., 2017). К тому же ТЭ может стать эффективным инструментом сокращения интервала между поколениями высокоценных животных.
С геномным анализом, выполненным вскоре после рождение, стало возможным рано определять генетическую ценность быка, и сразу после появления зрелой спермы использовать ее для процедур ЭКО. Ранняя геномная оценка молодых телок также позволяет начать производство от них коммерческих эмбрионов (Sirard, 2018) и ооцитов (Landry et al., 2016).

Число генотипированных животных, прошедших геномную оценку молочного скота в США
В США некоторые крупные молочные заводы уже обзавелись собственными (карманными) геномными лабораториями (!) и начали осуществлять собственную проверку лучших животные для размножения.
2. Повышение качества ооцитов, дело не одного Блондина (397). Качество получаемых in vitro ооцитов является главным фактором успеха (Lonergan and Fair, 2016). Потенциал яйцеклетки определяется ее способностью развиться до бластоцисты и в значительной мере обусловлен размером антрального фолликула (Lonergan et al., 1994), независимо от способов выращивания in vitro или in vivo (Rizos et al., 2002).
По мнению группы Блондина (Blondin et al., 2002) на этот потенциал можно воздействовать, изменяя период гормональной симуляции. Увеличение периода ФСГ стимуляции до 6-ти дней с последующей 48-часовой обработкой ЛГ за 5 часов до сбора яйцеклеток OPU позволили увеличить сбор бластоцист до 80% (Blondin et al., 2002).
Если же аспирация фолликулов применялась в случайные дни полового цикла (на разных стадиях развития фолликулов) 85% из них имели разную степень атрезии вследствие процесса апоптоза клеток (Hendriksen et al., 2000).
Синхронизация фолликулярных волн перед OPU обеспечивает увеличение скорости продуцирования эмбрионов и даже их приживляемость ТЭ (Cavalieri et al., 2018).
3. Сбор и качество ооцитов у телок и телят препубертатного периода (398). В последнее время наблюдается рост коммерческого интереса к производству эмбрионов крупного рогатого скота от препубертатных телок и телят-девочек. Интерес к селекции лучших животных в более молодом возрасте, преследует цель ускорить генетический прогресс за счет сокращения интервала между поколениями (Baldassarre et al. др., 2018).
Геномные технологии последних лет позволяют предсказать появление лучшего фенотипа сразу после рождения животного (Ponsart et al., 2013). В настоящее время, доступны небольшие ультразвуковые датчики OPU, которые позволяют производить эмбрионы IVP (in vitro) от молодых самок (Moore and Hasler, 2017).
Несколько исследований показали, что ооциты теленка имеют меньший потенциал для развития в полноценные эмбрионы по сравнению с ооцитами взрослых коров (Baldassarre and Bordignon, 2018), так как препубертатные самки имеют незрелый и нефункциональный гипоталамус, нерабочую ось гипофиз-яичники и яйцеклетки не достигают полного развития фолликулов до стадии овуляции (Sanchez and Smitz, 2012).
Тем не менее опыты показали, что телята голштинской породы в возрасте от 5 до 7 месяцев давали больше ооцитов, чем циклирующие телки 16-18 месяцев. Хотя процент развития зигот до бластоцист был выше у циклирующих телок, чем у телят, общее количество качественных эмбрионов (6–8 шт/гол) в итоге не отличалось (Landry et al., 2016). Можно сказать, что «подростковые» яйцеклетки, проигрывая в качестве ооцитов на начальной стадии, берут реванш за счет количества.
Таким образом, с появлением на комплексах геномного анализа, совершенствования в последнее время технологий ЭКО и высокого интереса производителей молочной продукции к использованию для производства эмбрионов элитных самок в максимально молодом возрасте (от 2 месяцев) дают уверенность, что очень скоро ЭКО станет обычной практикой для телятников высокопродуктивного скота. Вот такая детская «порнография» вероятно ждет и молочные комплексы России в ближайшее 3-5 лет.
4. Достижения в эмбриональных культуральных средах (398). Для производства эмбрионов in vitro (IVP), используют специальные среды для созревания и оплодотворения ооцитов «в пробирке», которые должны максимально имитировать физиологические этапы связанные с зарождением жизни в организме самки. У крупного рогатого скота примерно 90% незрелых ооцитов, извлеченных из фолликулов у доноров с неизвестным половым циклом (яичники из боен), продолжают созревание in vitro и около 80% из них подвергаются оплодотворению (Lonergan and Fair, 2016).
Используемые среды могут быть определяющим фактором в производстве и качестве бластоцист и криотолерантности эмбрионов (Sanches et al., 2013). Изменения последних лет в условиях культивирования, такие как добавление липолитического химического вещества и корректировка в концентрации плодной сыворотки теленка в средах были сделаны с целью увеличить крио-выживаемость эмбрионов (Sanches et al., 2017). В этом контексте, несколько исследователей предлагают использовать форсколин и феназина этосульфат (PES), как вещества, которое уменьшают накопление липида в клетках (Sudano et al., 2011; Paschoal et al., 2017).
Авторы оценивают результаты последних лет в улучшении питательных сред (добавление разных продуктов, цитокинов, ростовых факторов, антиоксидантов и других веществ) как скромные. Качественный сбор бластоцист in vitro до сих пор редко превышает 40–50% (Lonergan и Fair, 2016). Таким образом, пропорция ооцитов, развивающихся до стадии бластоцисты, остается схожей с периодом 1990-2000 гг., в котором оно достигло плато из 30-40% (Sirard, 2018). Скопировать природу матки и ее среду обитания пока получается плохо.
4. Использование разделенной спермы и ее преимущество (399). В промышленном молочном скотоводстве производство бычков является нежелательным. Однако исследования показывают, что выход sex-бластоцист при процедурах in vitro бывает ниже, в сравнении с использованием обычной спермы (Seidel Jr. 2014).
Тем не менее Cottle et al. (2018) выявлены превосходные результаты по прибыльности использования sex-спермы для планирования весенних отелов в Ирландии на высокопроизводительной ферме. Авторы заключают, что сексированная спермопродукция может быть использована на фермах с отлаженным воспроизводством к полному удовольствию владельцев.
Попробуем разобраться. В молочной промышленности избежать производство бычков, имеющих избыточный вес – это особенно важный вопрос (Holden, Butler, 2018). Использование спермы по половому признаку в репродуктивных биотехнологиях представляют собой значительный прогресс в мировом промышленном животноводстве, так как оно оптимизирует продуктивность и прибыльность молочного стада (Morotti et al. al., 2014). Среди репродуктивных биотехнологий наиболее частым применением спермы, разделенной по полу, является ЭКО, при котором может быть достигнуто хорошее количество однополых бластоцист на выходе (Matoba et al., 2014). Более того, для ЭКО требуется гораздо меньше сперматозоидов на ооцит, чем при ИО.
В США в 2016 г. более 90% из 4,5 — 5 миллионов соломинок разделенной по полу спермы было получено от быков-производителей молочных пород (Moore and Hasler, 2017). Однако исследования показывают, что выход бластоцист при использовании sex-спермы оказался ниже, чем при использовании обычной спермы (Seidel Jr. 2014).
Авторы пришли к выводу, что сексированная спермопродукция более подходит для хозяйств, которые уже имеют отличные показатели оплодотворяемости по стаду. И наоборот, такая техника производства sex-ориентированных бластоцист in vitro противопоказана для молочным хозяйств с неоптимальными показателями плодовитости стада (Cottle et al., 2018). То есть работает принцип: сложные технологии – для лучших.
В любом случае нацеленность на воспроизводство молочного стада желаемого пола животных (при ИО телок и традиционной ТЭ) оправдывает расширение использование спермы с разбивкой по полу.
5. Достижения в криоконсервации с использованием DT (С. 399). Несмотря на преимущества ЭКО, криоконсервация остается проблемой для коммерческих лабораторий (Sudano et al., 2011). Среди методов криоконсервации витрификация чаще используется во всем мире из-за хорошей скорости процедуры и низкой стоимости (Dode, 2013). Метод требует высокой концентрации криопротекторов и квалифицированного специалиста для оценки качества эмбриона, а главное для проведения сложных манипуляций, предшествующих витрификации (Vajta и Kuwayama, 2006).
Тем не менее упрощенный метод размораживания и прямой пересадки DT (Direct Transfer), хорошо известный специалистам традиционной ТЭ in vivo может стать хорошей альтернативой для коммерческого использования эмбрионов произведенных in vitro.
В исследовании Sanches et al., (2016) на помесных голштинских донорах (1/2) получены следующие показатели стельности после пересадки «пробирочных» эмбрионов:
- ТЭ свежих эмбрионов 51,35 ± 1,87% (133/259);
- ТЭ подвергшихся витрификации 35,89 ± 3,87% (84/234);
- ТЭ после медленного замораживания и прямой пересадки DT 40,19 ± 4,65% (125/311).
Автор делает вывод, что для промышленной технологии производства молока остается актуальным традиционное медленное замораживание и прямая пересадка (DT), которая не требует оценки зародышей после размораживания.
Заключение. Геномная селекция молодых животных + однополое семя + замораживание in vitro бластоцист для прямой ТЭ, открывают новую эру ЭКО в молочном секторе (Sirard, 2018). Однако, поскольку многие из этих процессов зависят от квалификации специалистов или даже от окружающей эмбрион среды, эта техника ЭКО остается пока доступной для производственников бизнес-класса. Тех, кто может позволить себе, как в США, организовывать собственные геномные лаборатории и внедрять собственные геномные тесты оценки и методы определения лучших воспроизводимых животных.
Стратегия увеличения производства эмбрионов in vivo и in vitro для ТЭ у крупного рогатого скота (с. 411)
В статье ученых из Аргентины, Эквадора и Канады (Саскачевань) указаны пути как можно подобраться к возможности суперстимуляции поливуляции. О решении этой проблемы мечтал и автор во второй части аналитического обзора, еще не зная о работе латиноамериканцев. Давайте вспомним материал от 8 августа с.г. [2].
«Наш прогноз. Возврат интереса к традиционной ТЭ может осуществиться, если биотехнологам удастся нарастить качественный эмбриосбор после суперовуляции в 2-3 раза и убрать тормозящее воздействие доминантного фолликула (или чего-то еще) на стимулированный фолликулогинез.
Да и рекордные суперовуляции в 40-60 эмбрионов и яйцеклеток за сбор, которые иногда удивляют эмбриологов – свидетельствуют о нереализованном потенциале яичников, которые пока находятся в заторможенном состоянии, даже несмотря на стимулированную гонадотропную полиовуляцию.
Предпосылки к неограниченной полиовуляции есть – число зачаточных оогоний в яичниках самки составляет несколько сотен тысяч и сходен по потенциалу со сперматогенезом. …Вот тут бы на фазе вторичного фолликулогенеза было бы целесообразно заблокировать атрезию фолликулов и получить урожай в несколько сотен ооцитов.
Кто возьмется разблокировать стимулированный филликулогенез и уровнять в правах мужскую и женскую способность производить гаметы?»
Нашлись же смельчаки, которые не посчитались с мнением академика Лысенко (см. эпиграф) и попытались со шприцом в руках «разблокировать стимулированный филликулогенез». Оказывается, автор был не одинок в своих фантазиях и их уже начали осуществлять латиноамериканцы и канадцы. Вот что значит интернационализм в науке, когда одинаковые мысли приходят эмбриологам разных континентам.
Синхронизация волны фолликулогенеза. В чем суть попыток управлять фолликулярной волной? Традиционный режим производства эмбрионов in vivo предваряют ежедневные (х 2) внутримышечные процедуры с введением ФСГ 4 или 5 дней подряд. Некоторые исследователи (Bó et al., 2008; García Guerra et al., 2012) показали, что созревание фолликулов и общий сбор овуляций могут быть улучшены у некоторых доноров, если инъекции ФСГ проводить в течение 6 или 7 дней (х 2).
Для техники in vitro производство эмбрионов по схемам суперстимуляции гонадотропинами до аспирации фолликулов (перед OPU) все еще обсуждается и является не таким однозначным в зависимости от того, к каким породам принадлежит донор яйцеклеток Bos taurus или Bos indicus.
Одновременное получение эмбрионов in vitro и in vivo подряд с одного и того же донора имеет важные практические последствия, потому что это потенциально увеличивает производство эмбрионы за короткий промежуток времени.
После аспирации фолликулов (OPU) применяют более длительное введение ФСГ для суперстимуляции, т.е. используют 5-6-ти дневный протокол вместо традиционного 4-дневного (х2). В этом исследовании, у доноров «раскручивали» фолликулярную волну введением 400 МЕ конского хориогонического гонадотропин (еСG) через 1 день после OPU с последующим 5-дневными инъекциями ФСГ (Cirit et al., 2019).
С этой же целью в Южной Америке применяют метод синхронизации фолликулярной волны введением донорам 2 мг бензоата эстрадиола (ЭБ) или 5 мг эстрадиол-17β и прогестерона с установкой устройства для его высвобождения P4 (50 — 100 мг) в течение 4 дней до начала инъекций ФСГ (Bó et al., 1996, 2002a; Bó and Mapletoft, 2014).
Тем не менее, эстрадиол во многих других странах мира оказался недоступен для производственного использования и потребовал поиска альтернатив, таких как удаление фолликулов или GnRH (обзор Bó и Mapletoft, 2014).
Попытки синхронизировать фолликулярную волну с GnRH были изначально неудачными, однако последующие разработки оказались более перспективными. В этих случаях ГнРГ был назначен к применению через 1,5-3,0 дня после установки интравагинального P4-устройства (с прогестероном), которое увеличивало LH-чувствительного фолликула к воздействию ГнРГ.
По той же теме работал Bó et al. (2010), который для синхронизации волны овуляции до начала введения ФСГ сообщил об использовании PGF2α, P4-устройства и GnRH.
В итоге персистентный фолликул был удален после окончания действия прогестинового устройства, введения PGF2α и инъекций ГнРГ через 7 дней. Стимулированная овуляция произошла у более чем 95% животных.
Попытки улучшения суперстимуляции (поиграемся с ХГк). Были предприняты попытки увеличить суперовуляторный ответ путем добавления хориогонического гонадотропина кобыл (eCG, ХГк) до начала введения ФСГ. Предварительная обработка ХГк за 2 дня до обычного введения ФСГ привела к численно большему количеству качественных эмбрионов (6,7 ± 1,2 против 4,9 ± 0,9) в группе обычных доноров (Caccia et al., 2000), и значительно больше эмбрионов извлекли у доноров, которые были определены как трудные на суперовуляцию (3,6 ± 0,6 против 1,0 ± 0,2; Bó et al., 2008).
В недавнем исследовании (García Guerra et al., 2012) оценили суперовуляторный ответ и качество эмбрионов у доноров с 4-х или 7-дневным введением ФСГ с использованием общей дозы 400 мг ФСГ (Folltropin-V; Vetoquinol Inc., Канада) два раза в день в постоянной суточной дозе. Среднее число больших фолликулов (≥ 10 мм) до овуляции в 7-дневной группе введения ФСГ составило 27,5 ± 4,1 против 19,5 ± 2,6 (P = 0,11), число овуляций, обнаруженных УЗИ также было больше (30,9 ± 3,9 против 18,3 ± 2,9, P = 0,01).
Причем овуляции происходили более синхронно в 7-дневной группе (93% овуляций произошли от 12 до 36 часов после пика ЛГ) по сравнению с 66% у 4-х дневной группе. Авторы считают, что в этих исследованиях определяющим фактором успеха суперовуляции была продолжительность введения, а не дозировка ФСГ.
ХГЧ вместо ФСГ. А вот применение одной инъекции ХГк в дозе 600 или 800 ИЕ вместо последних 4 введений ФСГ (2х2) с целью экономии ФСГ и увеличения ЛГ присутствия не привели к выгодам в суперовуляции 12 или 18 опытных доноров мясной породы бонсмара в сравнении с контролем. Но в то же время и не навредили: в первом опыте получен (что важно) одинаковый выход качественных зародышей на урезанной дозе ФСГ (5.3 и 5.7). Думайте сами – решайте сами, вводить или не вводить.
Эмбриопродуктивность доноров породы Bonsmana суперовулированных FSH или FSH+ eCG
| n | Общийэмбриосбор | Оплодотворенныхяйцеклеток | Качественных эмбрионов | |
| Эксперимент 1 | ||||
| ФСГ 300 мг | 12 | 11.7 | 10.5 | 5.7 |
| ФСГ 200 мг + ХГк 800 ИЕ | 12 | 9.6 | 6.8 | 5.3 |
| Эксперимент 2 | ||||
| ФСГ 200 мг + ХГк 600 ИЕ | 18 | 6.7 | 5.4 | 3.6 |
| ФСГ 200 мг + ХГк 800 ИЕ | 18 | 6.1 | 4.3 | 3.7 |
Надо добавить, что описанные 4-х дневные суперовуляции доноров проходили в фиксированное время по программе ТЕТ-д на фоне действия внутриматочного имплантанта с прогестероном (Р4). При его введении дополнительно использовали инъекцию эсьтрадиола-17β (ЕВ). Все доноры получили 2-х кратную инъекцию PGF2α на 3-й день обработки.
Стратегия ТЭ реципиентов в фиксированное время (ТЕТ-р). Применение программы с использованием синхронизации течки и овуляции реципиентов предназначены для снятия ограничений, связанных с обнаружением охоты и были изначально разработаны для ИО в фиксированное время (TAI), а затем применены для реципиентов с фиксированным сроком пересадки (TET; Bó et al., 2002, 2012).
Схемы синхронизации реципиентов для ТЕТ обычно делятся на те, где инициацию фолликулярной волны осуществляют рилизинг-гормонами гипоталамуса (ГнРГ; Ambrose et al., 1999) и те, в которых с этой целью применяют эстрадиола бензоат (ЕВ; Bó et al., 2002). Инъекции проводят на фоне 4-5 дневного воздействия устройства, содержащего прогестерон, например Sidr (P-4). После его удаления реципиенту вводят хориогонический гонадотропин лошади (eCG) + простагландин Ф2а (PGF2а). Выбор схем синхронизации часто связан с наличием гормонов в разных странах и разрешением на их использование.

A) Модифицированный 5-дн протокол ТЭ в фиксированное время (TЕT): ±GnRH+P4 устройство на День 0, PGF2а + eCG на День 5 и GnRH на День 8. ТЕТ на 15 день протокола.
B) J- Synch протокол: EB+ P4 на День 0, PGF2а + eCG на День 6, GnRH on Day 9. ТЕТ на 16 день.
Если обнаружение течки происходит с помощью выявления охоты или окраски хвоста, реципиентов наблюдают через 72 часа после удаления P4 в протоколах A и B.
P.S. от автора.
В этом материале описана методика коммерческой ТЭ в фиксированное время для реципиентов (ТЕТ-р), а в предыдущем – суперовуляция и ТЭ в фиксированное время на фоне синхронизации овуляции и одновременной суперовуляции коров-доноров (TET-д). В этих материалах, к сожалению, не приведены результаты вымывания и пересадки эмбрионов после таких манипуляций с реципиентами.
Чтобы не случилось ситуации (см. эпиграф) — коров на мясо, эмбриологов под арест… домашний — все эти многоходовые схемы синхронизации и супепровуляции надо проверять на ограниченном поголовье.
Не надо забывать, что четкую фиксацию желтого тела у реципиентов при самых крутых схемах ТЕТ никто не отменял.
И если методика ТAI (ИО без выявления охоты) достаточно отработана, то в отношении ТET авторы обзора поясняют, что «…optimal P/ET and calving rates were obtained when tail paint was used to detect estrus and only recipients with their tail paint rubbed-off (i.e., in estrus) received embryos 7 days later».
То есть лучшие результаты были получены у реципиентов, которых после синхронизации овуляции и за 7 дней до TЭ все-таки наблюдали в охоте.
То же, на взгляд автора. касается и использования «овсинга» и прочих «синков» в схемах суперовуляции, которая может выглядеть следующим образом.

Продолжительность этой программы стимулированной суперовуляции составит 30-32 дня и может войти в арсенал эмбриологов после производственной проверки.
Можно ли сократить интервал синхронной подготовки доноров к извлечению эмбрионов? С этой целью может быть применена схема 9-ти дневного воздействия средства, выделяющего прогестерон (CIDR, PRID, Crestar). На 6-ой день прогестероновой блокады проводится курс ФСГ-суперовуляции продолжительностью 4 или 5 дней. На 9-й день одновременно с удалением средства Р4 донору вводиться простагландин Ф2a (для удаления желтых тел) и хоригонический гонадотропин (средство стимуляции овуляции). Искусственное осеменение доноров по приходу в охоту на 10-13 день, извлечение эмбрионов на 18-20 день.

В этой схеме, когда доноров запускают в суперовуляцию без выявления охоты и наличия желтого тела используют три средства синхронизации овуляции: прогестероновый фон (на 9 дней), хориогонический гонадотропин, стимулирующий выброс ЛГ (при отсутствии у доноров желтых тел) и простагландин Ф2a (для коров с желтым телом в яичнике).
Умелые ручки или необычное использование ТЭ
Мы привыкли, что традиционно ТЭ применяется в молочных стадах для воспроизводства животных с высоким генетическим потенциалом, но приведенные исследования показывают, что метод может применяться еще и как лечебное средство для улучшения репродуктивной способности высокопродуктивного коммерческого стада. Основное поле деятельности для этого потенциального улучшения заключается: 1) в борьбе с тепловым стрессом в сезоны тепловых нагрузок и 2) в терапевтическом повышении фертильности коров после переноса эмбрионов у коров «перегульщиц».
О такой возможности борьбы с тепловым стрессом, впервые нашедшей свое применение в практике российской эмбриологии (Кубанский молочно-товарный комплекс) мы подробно писали в первой части обзора [1].
Автор — страшный человек! Выполнил годовой объем исследовательской работы полноценной лаборатории репродуктивных технологий НИИ животноводства.
Алекскандр Дуванов: «Пересадки сексированных эмбрионов коровам, да еще в период жары – это элементарно! Как два пальца…»
«Оказалось, что тепловой стресс губителен для оплодотворения зародышей в матке доноров или in vitro, но не способен в такой же степени влиять на прикрепление его к матке реципиента и установлению стельности. То есть производить эмбрионы следует в комфортных условиях для донора, а выполнять пересадки реципиентам оттаянными зародышами не возбраняется и в сезон тепловых нагрузок.
В условиях Кубани в июле-сентябре эффективность ИО коров снижается в 3 и более раз до 12-17%. Авторы статьи сумели удержать планку стельности коров-реципиентов на приличном уровне стельности (42.9%) в жаркий период года за счет пересадки замороженно-оттаянных эмбрионов и даже в 3 раза улучшить показатели стельности по стаду в сравнении с ИО (!).
К тому же сумели заложить почти 43% стельности «женскими» сексированными эмбрионами после их пересадки, в то время, когда даже полноценная несексированная спермопродукция после ИО дала на коровах КМТК всего 16% стельности. Напомним, что сексированная спермопродукция на коровах в любое время года для ИО не применяется из-за низкой эффективности покрытия».
Так что борьбой с тепловым стрессом и дамским угодничеством (в отношении «женской» спермы), нас не удивишь. Латиноамериканцы в своей статье лишь упоминают о потрясающей (так в тексте) возможности бороться с тепловым стрессом коров и попутно производить из эмбрионов женское потомство, т. е. получать и высаживать сексированные по полу эмбрионы.
Наш краснодарский коллега Дуванов А.В. успешно применяет эти два приема уже в течение 2-х лет. Элементарно, как два пальца…
Еще одна альтернатива, упомянутая в статье заключается в использовании эмбриотерапии для повторно покрываемых коров.
Коров-«перегульщиц» обычно определяют как животных, которые не забеременели в течение определенного периода времени (обычно после 3 или 4 неудачных ИО), не имеющих явных отклонений в репродукции, которые могут быть диагностировано при ветеринарном осмотре.
В исследовании Rodrigues et al., (2007), темпы закладки стельности коров «повторок» голштинской породы были выше после ТЭ in vivo (41,7%; 1609/3858), чем после ИО (17,9%; 1019/5693). Такой результат авторы статьи объясняют тем, что проблема фертильности у некоторых высокопродуктивных «повторок» может быть связана с качеством ооцитов и/или в сбое раннего развития эмбриона. Другие отчеты также показали значительное улучшение показателей беременности у коров-«повторок» с использованием техники ТЭ in vivo (Son et al., 2007; Dochi et al., 2008) или in vitro (Block et al., 2010). В последнем случае для производства эмбрионов достаточно использовать лишь одну соломинку спермы (Pellegrino et al., 2016).
И по этой теме врачевания копров с использованием ТЭ Александр Дуванов и Николай Хромов из КМТК не уступает латиноамериканцам.
Приводят данные по применения пересадки сексированных эмбрионов на коровах с хроническим бесплодием (более 200 дней), выполненных в период теплового стресса.
Приживляемость сексированных эмбрионов у коров-реципиентов с разными сроками бесплодия на КМТК в период теплового стресса (июль-сентябрь 2019 г.) и в сравнении с искусственным осеменением коров (Дуванов А.В. , неопубл.)
| Дней бесплодия коров до результативной ТЭ | ИО | |||
| до 200 дн | >200 дн | В среднем | ||
| Пересадок | 541 | 116 | 657 | 2202 |
| Стельных | 212 | 35 | 247 | 464 |
| % | 39.2 | 30.2 | 37.6 | 21.1 |
Треть коров «перегульщиц» со сроком яловости более 7 месяцев (!) удалось вернуть в производственный цикл в период теплового стресса и низкой эффективности искусственного осеменения по стаду. К тому же обеспечить их женским приплодом от более удачливых подруг-доноров. Вот что может современная ТЭ в умелых руках!
Заключение. В настоящее время производство эмбрионов in vivo и in vitro можно комбинировать с эффективной синхронизацией в программах TAI и TET. Если ранее технология переноса эмбрионов много лет широко использовалась в молочных стадах, в основном с целью генетического улучшения ограниченного поголовья высокопродуктивных коров-доноров, теперь техника ТЭ может быть использована для решения репродуктивных проблемы, таких как снижение фертильности в летние месяцы и у коров — «повторок».
Витрификация (c.431).
В биологии остекленение называют витрификацией, она с успехом используется в медицине для криоконсервации эмбрионов человека, но пока никак не приживется на фермах. Витрификация – дама хотя и капризная (см. таблицу), но похоже за ней будущее.
Эмбрионы коров in vivo никак не хотят ей покоряться и имеют большой разброс стельности реципиентов (17.8 – 46.7%) в сравнении с традиционным медленным замораживанием (19.5 – 59%). С ней, по этому поводу, смог договориться лишь эмбриолог с героически не выговариваемой фамилией van Wagtendonk-de Leeuw, достигший на 393 зародышах стельности в 44.5% (в контроле 45.1%).
Выживаемость эмбрионов крупного рогатого скота, полученных in vivo, после медленного замораживания и витрификации
| Размер стельности (%) | |||
| Медленное замораживание | Витрификация | Р- значение | |
| Massip et al., 1987 | 51.8 (n = 27) | 39.1 (n = 23) | >0.05 |
| van Wagtendonk-de Leeuw et al., 1995 | 59 (n = 40) | 43 (n = 34) | 0.10 |
| van Wagtendonk-de Leeuw et al., 1997 | 45.1 (n = 335) | 44.5 (n = 393) | 0.79 |
| -˶- | 19.5 (n = 79) | 17.8 (n = 73) | >0.05 |
| Mattos et al., 2010 | 29.8 (n = 102) | 36.6 (n = 100) | >0.05 |
| Inaba et al., 2011 | 45.2 (n = 62) | 46.7 (n = 30) | >0.05 |
Что удивительно, эмбрионы IVP (in vitro) дают более удовлетворительные результаты при витрификации, чем полученные in vivo. Эту особенность первыми обнаружили медики, где витрификация превалирует над другими способами замораживания. Криоконсервирующая среда подвергается прямому переходу из жидкого в остеклованное и аморфное состояние без кристаллизации, благодаря большой вязкости криоконсервирующей среды и высокой скорости замерзания (> 20.000 °C/мин) путем прямого погружения эмбрионов в N2 от комнатной температуры. А что потом — после их оттаивания — можно посмотреть на фото.
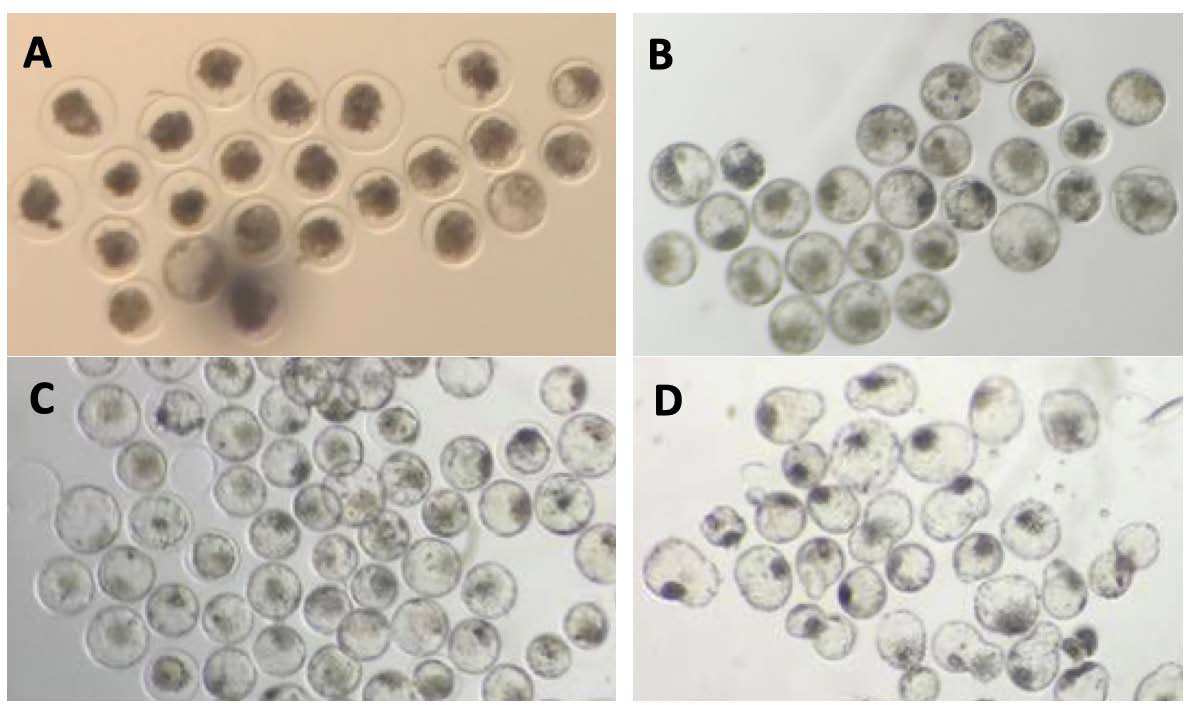
Витрифицированные in vitro эмбрионы крупного рогатого скота.
Сразу после оттаивания (A), а также через 6 ч (B) и 12 ч. культивирования: экспандированные (С) и выходящие из зоны бластоцисты (D)
Для обеспечения быстрой скорости охлаждения, используют минимальный объем раствора. С этой же целью применяют специальные инструменты, способствующие упаковке эмбрионов в микрокапли, такие как открытая вытянутая пайетта (OPS) (Vajta et al., 1998), Cryoloop (Lane et al., 1999) и Cryotop (Kuwayama, 2007).
Совсем недавно была предложена новая автоматизированная методология витрификации (Arav et al., 2018), которая может облегчить и оптимизировать стандартизацию техники криоконсервации.
Мы с вами бегло просмотрели примерно половину статей, где есть предпосылки для выхода эмбриотрансфера на производственный уровень. А еще в сборнике есть информация по пересадкам эмбрионов у других животных, короткие сообщения (аннотации) из разных уголков мира, занимающие в общей сложности половину печатного объема сборника.
По-прежнему много материала по теории ТЭ и статей поискового плана. Есть даже попытки «вселенского» анализа для специалистов, мыслящих глобально. Хотите объять необъятное? — см. стр. 508 сборника и рисунок в приложении.
Статья называется «Ооциты, эмбрионы и плюрипотентные стволовые клетки с биомедицинской точки зрения». Может у кого-то получиться разобраться в этой «Биомедицинской Круговерти» европейских исследователей (картинка в приложении).
От себя могу добавить, что уровень квалификации специалистов работающих по программам ТЭ in vitro можно сравнить с подготовкой IT-специалистов в компьютерном программировании. В отличие от последних – они программируют жизнь высокопродуктивного поголовья и работают по общебиологическим принципах, одинаковых для всех млекопитающих, включая человека. Куда тем айтишникам с их программами до биологических программ зарождения жизни, которые приходиться разрабатывать эмбриологам, чтобы пытаться скопировать природные закономерности эмбриогенеза.
Ссылки и библиография.
- https://www.dairynews.ru/news/transplantatsiya-embrionov-2019.html
- https://www.dairynews.ru/news/transplantatsiya-embrionov-2019-2-probirka-ili-tra.html
- https://www.dairynews.ru/news/transplantatsiya-embrionov-2019-3.html
- http://www.dairynews.ru/news/transplantatsiya-embrionov-brazilskiy-fenomen.html
- http://www.sbte.org.br/arquivos/anais/Proceedings_SBTExAETE_2019_1.pdf
- https://www.dairynews.ru/news/primenenie-tekhnologii-transplantatsii-embrionov-d.html
- Мадисон В.В. Трансплантация эмбрионов племенного скота // Животноводство России. — 2011. — №10. — С.8-10
- http://www.madison.pp.ua/rf-chelyabinskie-peresadki-embrionov-iz-kanady
- http://bredynews.ru/novosti/selskoe-khozyajstvo/2413-elitnyj-skot-iz-ooo-agrofirma-kalininskaya-polzuetsya-sprosom-po-vsej-strane
- https://ruminants.msd-animal-health.ru/schemes/gormonalnye-skhemy/?utm_source=google&utm_medium=cpc&utm_campaign=schemes&utm_content=gormonalnye-skhemy
- Мадисон В. Синхронизация охоты крупного рогатого скота препаратами ПГФ-2& // Молочное и мясное скотоводство. — 2000. — № 7. — С.9-14
- http://www.dairynews.ru/news/etapy-proydennogo-puti.html?sphrase_id=535712
- http://orensau.ru/ru/novosty/5/6542-konferentsiya-po-transplantatsii-embrionov

«Oocytes, embryos and pluripotent stem cells from a biomedical perspective» (с. 508)
Автор: Виктор Мадисон, канд. биол. наук, г. Новочебоксарск
